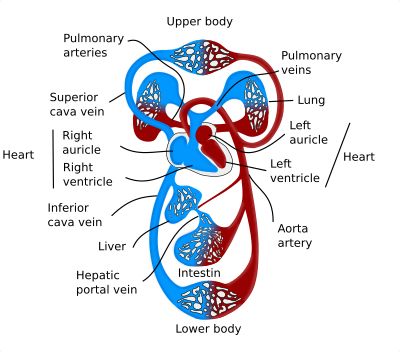
Aparatul circulator poate fi impărţit în trei mari componente:
- inima,
- vasele sanguine şi
- sângele.
Acestea sunt strâns legate între ele şi afectarea unei componente va atrage în scurt timp dereglarea celorlanîi parametri de circulaţie. De exemplu, dacă conţinutul de potasiu din sânge scade, cum se poate întâmpla în tratamentul cu glicozizi şi cordul mai este susţinut şi cu diuretice tiazidice va fi urmat de posibila creştere a efectului negativ al glicozidelor pâna la fibrilaţia ventriculară.
În acelaşi mod, dacă, în cazul şocului, vasele periferice se dilată, atunci rata bătăilor cordului va creşte, iar la arteriole se va instala constricţia ca mecanism regulator reflex în intenţia menţinerii unei presiuni constante a sângelui în vase.
În acelaşi timp, vasele dilatate vor favoriza pasajul lichidelor din sânge spre spaţiul tisular, astfel scăzând volumul circulant vascular şi creşterea componentei celulare şi instalarea hemoconcentraţiei sângelui. Presiunea sângelui va fi menţinută constantă de către cord care va regla rata volumului pompat într-un sistem distribuţiereîntoarcere a sângelui cu un volum fix. Presiunea poate fi scăzută prin patru mecanisme:
- scăderea volumului de sânge pompat în cord/minut (minut volumul cardiac),
- scăderea volumului sângelui (prin hemoragie),
- creşterea vâscozităţii sângelui (prin hemoconcentaţie) şi
- creştere volumului spaţiului circulator (prin vasodilataţie).
În condiţii homeostatice normale presiunea ar trebui să rămână optimă, atacul cardiac fiind dependent de presiunea care va putea forţa ventriculele (aceasta fiind dependentă la rândul ei de gradul de compensare artrial). Returnul venos va depinde de acea presiune arterială care va conduce sângele în venule presiunea cardiacă este reglată reflex de către arcul aortic şi de către senzorii carotidieni via centrii medulari vitali şi de către sistemul nervos autonom.
Volumul sanguin şi gradul hemoconcentraţiei sunt menţinute constant de către mecanisme legate de renină/angiotensină/aldosteron, prin acţiunea aldosteronului sau prin acţiunea hormonului antidiuretic asociată cu activitatea factorilor natriuretici (aceste peptide relaşate de muşhiul atrial). În acest mod cordul are şi activităţi regulatoare endocrine. În întâmpinarea acestei integrări multe medicamente care acţionează asupra cordului vor acţiona şi asupra sistemului vascular într-o manieră directă sau indirectă.
Cea mai potivită categorie de medicamente va fi aleasă de către natura malfuncţiei instalate (de exemplu simpaticomimeticele se vor administra pentru a corecta căderea presiunii sanguine care se poate instala în urma anesteziei epidurale când căile simpatice sunt blocate). Totuşi, nu întotdeauna problemele circulatorii pot fi rezolvate aşa de simplu şi utilizarea medicamentelor în situaţii complexe cum este şocul solicită o evaluare atentă.
Medicamentele sistemului circulator se clasifică în:
- cardioexcitante,
- simpaticomimetice,
- vasoconstrictoare,
- asistolice,
- vasodilatatoare şi
- hemostatice.
1. Bazele fiziologice ale terapiei cordului
Considerăm că pentru a înţelege modul de acţiune al medicamentelor asupra cordului se impune o foarte scurtă rememorare, farmacodinamia medicamentelor acestui sistem fiind foarte influenţată şi legată de fiziologia organului.
Celulele muşchiului cardiac se contractă spontan datorită proteinei contractile specifice, actomiozina şi datorită sistemului (mitocondrial) energo-generator limitrof.
Contracţia va fi realizată de către ionii de calciu, eliberarea lor fiind ciclică după depolarizarea membranară (care va precede fiecare contracţie).
Această activitate electrică este reversibilă. Ea va permite permeabilizarea membranei şi pătrunderea ionilor de sodiu şi eliberarea celor de potasiu şi mai apoi pătrunderea calciului, via canalele ionice voltaj/dependente, în funcţie de gradientul de concentraţie.
Acest flux determină inversarea polarităţii electrice a membranei cardiace care va fi adusă în final la nivelul de echilibru (de – 80 la – 90 de milivolţi, odată cu ieşirea ionilor de Na+ în schimbul celor de K+ ) în timpul perioadei refractare.
Ritmicitatea cardiacă este determinată de către nodul sino-atrial datorită celulelor care polarizează/depolarizează în mod spontan şi mult mai frecvent decât oriunde în cord.
Din acest considerent celulele nodului îşi vor impune amprenta asupra întregului organ prin conductanţă electrică.
Potenţialul de acţiune va creşte concentraţia ionilor de calciu din celule; acestea vor cupla la troponină, miozin-ATPaza va fi activată şi astfel ATP-ul va fi hidrolizat. Ca urmare, se vor forma legăruri (încrucişate)de actină-miozină şi celula cardiacă se va contracta. Relaşarea contracţiei se va realiza prin înlăturarea ionilor de calciu prin mecanisme specifice (polimerizarea-depolimerizarea tubulinelor). Datorită inervaţiei duale, simpatice şi parasimpatice, nodul sino-atrial va fi influenţat de preponderenţa uneia sau alteia.Astfel, nodul va fi supresat de către curenţi K+ - acetilcolin hiperpolarizanţi care vor diminua generarea ratei acţiune-potenţial care funcţional vor antrena scăderea forţei de contracţie a cordului.
Atropina poate bloca coliniceptorii muscarinici nodulari şi astfel, eliberează nodul sino-atrial de influenţa frenatoare a vagului. Acest fapt va fi urmat de cresterea ritmului cardiac datorită dominaţiei preponderente a parasimpaticului.
1.1. Corelaţia: receptori, mesageri secundari şi acţiunea medicamentelor
Cordul posedă ά-, dar mai ale βadrenoreceptori, activarea lor fiind urmată în principal de pătrunderea într-o rată crescută a ionilor de Ca+ în celula cardiacă, consecutiv cu creşterea contracţiei şi mai apoi de relaxarea musculaturii cardiace.
Când β-adrenoreceptori sunt activaţi, aceştia vor creşte rata şi forţa contracţie cordului, care este precedată de către creşterea concentraţiilor intracelulare de AMP-c (adenozin-monofosfat ciclic).